趨勢觀察:生命科學領域倫理治理現狀與趨勢
|
|
中國網/中國發展門戶網訊 生命科學是21 世紀發展最為迅速的學科領域之一,其新成果、新技術不斷涌現,為人類社會帶來了巨大的進步。同時,由于直接與“生命”密切相關,倫理問題也受到廣泛關注,甚至誕生了專門研究生命科學領域人類行為道德哲學和倫理規范的學科——“生命倫理學”。本文關注生命科學領域的熱點突破及其引發的倫理問題討論,簡要梳理各國涉及生命科學相關倫理問題的法律、法規、指南等治理規制,通過研判我國在生命科學領域相關倫理體系建設和舉措,針對存在的問題和挑戰,提出關于我國生命科學領域倫理治理的思考和建議。
生命科學領域倫理治理的總體態勢
生命科學領域每一項突破性技術的誕生,如1998 年首次成功分離并體外培養人類胚胎干細胞、2010 年首個“人工合成生命細胞”的誕生、2015 年 CRISPR 基因編輯技術首次應用于人類胚胎編輯、2021 年成功在人體上進行豬腎移植試驗等,都引發了人們對相關倫理和社會問題的廣泛關注,并由此推動或促進全球各國倫理治理體系的建設,包括相關法律法規的出臺和優化,以及相關倫理審查體系的完善等。然而,總體來看,生命科學領域相關倫理研究存在時滯性,且研究力度遠遠追不上科學研究快速發展的腳步。
生命科學領域新技術發展加速,相關倫理問題持續引發關注
從試管嬰兒到輔助生殖,從胚胎干細胞到人體克隆,從合成生物到基因編輯胚胎,每當生命科學領域產生突破性的成果,并展現出巨大應用潛力時,都會基于各自不同的科學原理和應用場景引發一系列倫理問題討論。
以基因編輯技術為例,雖然該技術的潛在科學價值已經得到廣泛肯定,但其復雜的倫理和安全爭議問題始終處在輿論熱點。由于作用對象的復雜性、技術本身的敏感性,以及對健康、環境、經濟、社會等方面影響存在的諸多不確定性及非預期效應,基因編輯可能引發的倫理風險是多層面的。隨著 CRISPR-Cas9 為代表的基因編輯技術研究的深入,科學家們開始嘗試在人類卵細胞、精子甚至胚胎上進行試驗,基因編輯技術的倫理問題更加引人注目。尤其是2018 年世界首例“基因編輯嬰兒”在中國誕生,引起國內外學術界和社會的廣泛關注,引發基因編輯技術倫理和監管問題的巨大爭議,更將基因編輯的倫理憂慮推上了高峰。同時,基因編輯技術可能帶來的生物安全問題也吸引各方關注。例如,2016 年《美國情報界年度全球威脅評估報告》將“基因編輯”列入“大規模殺傷性與擴散性武器”威脅清單,認為這種有雙重用途的技術分布廣泛、成本較低、發展迅速,任何蓄意或無意的誤用,都可能引發國家安全問題。
除了基因編輯技術,跨物種嵌合體研究進展迅速,倫理問題持續引發爭議。由于全球器官移植資源極度缺乏,通過將人的多能干細胞植入其他動物的胚胎,在嵌合體上“養出”人類器官跨物種嵌合體,培養獲得所需器官,成為再生醫學領域最具吸引力的技術。早在2016 年 Science評選出的20 大技術預測中,人類與動物的嵌合體技術就位列其中。2019 年11 月底,全球首例“豬猴嵌合體”誕生;2021 年,全球首個“人猴嵌合體”胚胎誕生,揭開了人胚胎著床后發育的“黑匣子”。
盡管跨物種嵌合體研究蘊含重大價值,但也潛藏著巨大的倫理風險,其中爭議較大的是嵌合體研究的邊界問題。有學者認為,生殖細胞和神經細胞是人類-動物嵌合體的倫理界限。美國、西班牙等國家認為只要嵌合體不具備繁衍能力且不會發育出大腦,即可允許制造人-動物嵌合體。針對“人猴嵌合體”的研究,我國動物學家季維智認為,人猴嵌合胚胎絕不是人猴雜交——人猴嵌合胚胎是把猴子胚胎作為人干細胞發育的環境,本質上并未發生生殖嵌合,并不有悖倫理。西班牙發育生物學家阿方索·馬丁內斯·阿里亞斯認為,相比猴子,用牛與豬來做研究“更具潛力,且不會有挑戰倫理邊界的風險”。同時,科學家們也強調,目前的研究只是停留在體外實驗的階段,如果人與動物嵌合體進入了體內實驗,植入到動物體內,最后發育成某種生物,則后果不堪設想。
全球各國加強治理體系建設,不斷達成倫理共識
生命科學領域顛覆性的新成果、新技術在帶給人類進步的同時,都會引發人們對可能出現的潛在倫理和安全風險的思考和探討,從而促使國際社會在生命科學領域的倫理治理方面不斷進步和完善(圖1)。
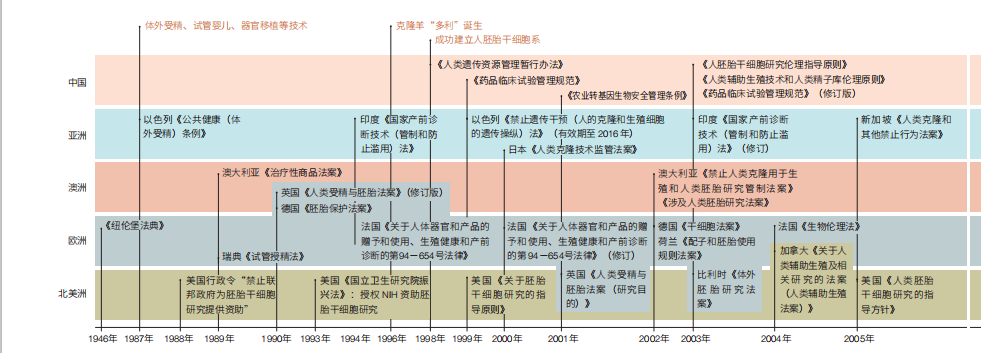

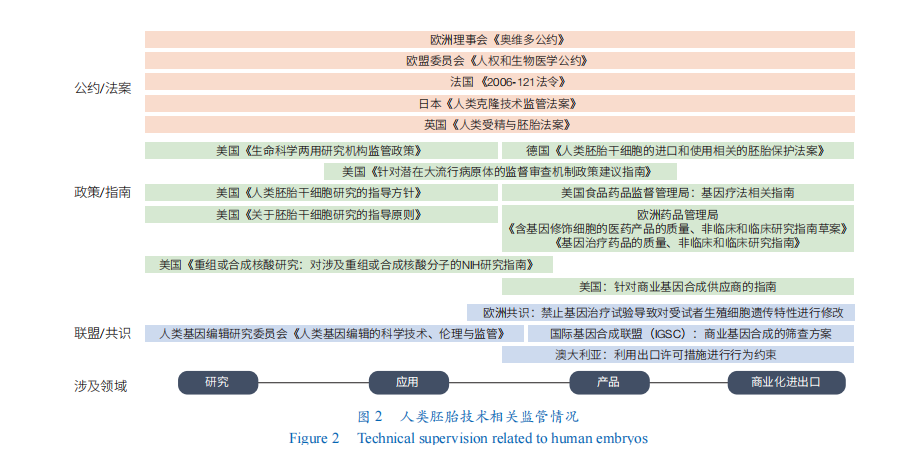
在新的技術風險出現時,各國基于本國的法律制度、歷史傳統和宗教信仰,紛紛制定了本國的生命科學領域倫理相關法律規定。尤其是對于干細胞和基因編輯等可能直接改變物種的新技術,世界各國已經通過多種措施監管和防范相關倫理問題,著力點主要在于涉及人類胚胎的科學研究管理、技術應用、操作規范,以及含有基因修飾或人工合成組分的醫學產品的管理、商業化和進出口等多個層次(圖2)。
1946 年在德國紐倫堡軍事法庭上誕生的《紐倫堡法典》,明確了醫生進行人體試驗的10 條標準,開辟了人體試驗規范化的先河。英國《人類受精與胚胎學法案》(1990 年發布,2008 年修訂)是全球第一部涉及人類胚胎的相關監管法案;其修訂版允許人類和動物“細胞融合”以創新“混合胚胎”的實驗,對后續干細胞技術的研究發展有所促進。德國《胚胎保護法案》(1991年發布,2012 年修訂)嚴格禁止人類胚胎干細胞研究及克隆胚胎干細胞;而德國《生殖醫學法(草案)》(2000 年發布)再次強調在德國不允許進行胚胎干細胞的培養研究。日本2014 年起實施《再生醫療安全性確保法》,將使用誘導多功能干細胞和胚胎干細胞的臨床研究和治療劃分為危險性最高的“第一類”,需由專門委員會進行審查。
除了國家層面的法律法規,各大國際組織紛紛出臺各類指南或管理框架,通過實踐指導,助力于科學共同體達成共識、自覺自治。例如,1964 年國際醫學大會通過的《赫爾辛基宣言》規定在人體醫學研究中,對受試者健康的考慮應優先于對科學研究的興趣,這為臨床研究倫理道德規范奠定基石;國際醫學科學組織理事會(CIOMS)于2016 年制定修訂版《涉及人的健康相關研究國際倫理準則》,旨在從倫理學、醫學產品開發及安全性方面來指導健康研究,促進公眾健康;國際干細胞研究學會(ISSCR)于2021 年5 月發布更新版《干細胞研究和臨床轉化指南》,有機結合了基于干細胞的胚胎模型、人類胚胎研究、嵌合體、類器官和基因編輯等領域最新研究進展與臨床倫理規范,為科學監管干細胞臨床轉化提出了切實可行的建議;2021 年7 月12 日,世界衛生組織(WHO)下屬專家委員會發布《人類基因組編輯管治框架》和《人類基因組編輯建議》,首次提出了將人類基因編輯作為公共衛生工具的全球建議,并論證了其安全性、有效性和倫理問題。
此外,國際社會也保持對生命科學領域突發事件的關注,積極應對可能出現的風險。聯合國教科文組織國際生物倫理委員會(IBC)和世界科學知識與技術倫理委員會(COMEST)聯合發布的《關于新型冠狀病毒肺炎的聯合聲明:全球視角下的倫理考量》表明,新冠肺炎疫情全球性大流行,急需全球生物倫理學的反思與應對。
我國生命科學領域倫理治理現狀
生命科學領域倫理問題研究日益受到重視
國家/地方多項基金、計劃支持生命科學倫理問題、政策和監管研究。國家社會科學基金項目2006 年以來資助生命科學領域倫理問題、法規、標準研究等相關項目超60 項,包括重大項目5 項、重點項目1 項。國家重點研發計劃等科技類資助項目中設置配套課題支持倫理相關軟科學研究,如2017 年精準醫學研究專項項目“精準醫療倫理、政策法規框架研究”、2018 年合成生物學專項項目“合成生物學倫理、政策法規框架研究”等。
近年來我國生命科學倫理相關研究論文日益增長。截至2021 年8 月,中國學者參與發表在 Web of Science 核心合集的生命科學倫理英文文獻96 篇,發表在中國知網(CNKI)的相關中文論文共1 290 篇;主要研究機構有中國科學院科技戰略咨詢研究院、北京干細胞與再生醫學研究院科技倫理研究中心、華中科技大學生命倫理學研究中心、復旦大學哲學學院等,主要研究內容包括生命科學領域新技術、新理念、新應用相關的倫理爭議、倫理反思、倫理審查、法律規制等。
社會各界不斷呼吁要正視生命科學領域的倫理問題,加強倫理監管。2018 年中國科學技術協會生命科學學會聯合體發表聲明,堅決反對有違科學精神和倫理道德的科學研究與生物技術應用;2019 年5 月,我國4 位倫理學家在 Nature上發表評論文章,呼吁加強對生物醫學研究的倫理監管,并提出重建我國科技倫理治理體系的6 個方面政策建議;2019 年和2021 年全國兩會上多位代表強調要重視生命倫理規范,建議要加強立法來引導、約束生命科學領域科研活動,提高處罰力度。
倫理相關法律法規相繼出臺,監管制度發展與時俱進
我國逐漸重視生命科學領域倫理監管,出臺多項新興技術應用的倫理監管舉措。《人胚胎干細胞研究倫理指導原則》(2003 年)、《涉及人的生物醫學研究倫理審查辦法》(2016 年)、《人體器官移植條例》(2017 年)、《醫療技術臨床應用管理辦法》(2018 年)、《醫療糾紛預防和處理條例》(2018 年)、《生物醫學新技術臨床應用管理條例(征求意見稿)》(2019 年)等政策法規對相關研究和臨床活動進行倫理約束,禁止不符合倫理規范的研究和實踐活動。
生命科學領域倫理相關立法層次逐漸提高。近年來,生命科學領域相關倫理規范逐步被寫入《中華人民共和國基本醫療衛生與健康促進法》《中華人民共和國民法典》《中華人民共和國生物安全法》《中華人民共和國刑法》等法律法規,尤其值得一提的是2020 年《中華人民共和國刑法修正案(十一)》新增非法進行人類基因編輯、克隆罪,明確了國家對于非法進行人類基因編輯、克隆行為的監管立場。這些法律條款從總體國家安全法律體系下,對生命科學領域的倫理監管與治理進行宏觀指導和規范,對生物技術研究、開發與應用活動、生物醫學臨床研究設立了明確的倫理規范要求——不得危害人體健康,不得違背倫理道德,不得損害公共利益。
倫理審查規定不斷更新,多層級倫理審查機構建設逐漸完善
涉及人的生命科學與生物醫學研究倫理審查制度不斷更新。《涉及人的生物醫學研究倫理審查辦法》(2016 年)已建立了較為系統的涉及人的生物醫學研究的倫理審查制度,規定了涉及人的生物醫學研究倫理審查原則,各級倫理委員會的設置和職責,倫理審查的程序、方法,以及審查的監督與管理等。2021 年4 月,國家衛生健康委員會結合新的形勢和要求,會同有關部門起草了《涉及人的生命科學和醫學研究倫理審查辦法(征求意見稿)》,將適用對象由生物醫學研究擴展至生命科學和醫學研究;更新立法依據,強調人的尊嚴、隱私保護,強化知情同意;并強調對于公共利益的保護。
多層級倫理審查機構建設逐漸完善。隨著相關政策及管理辦法相繼發布,我國的生命科學倫理審查委員會及相關獨立機構建設逐漸完善。對于涉及人的生物醫學研究領域形成了國家醫學倫理專家委員會、省級醫學倫理專家委員會和機構倫理委員會3 個級別的醫學倫理審查結構。此外,各省級衛生行政部門設立本行政區域的倫理審查指導咨詢組織,由此出現了新類型的倫理委員會,如生殖醫學倫理委員會、人體器官移植技術臨床應用與倫理委員會;各省市和地區相繼成立了多個區域倫理委員會,以滿足不具備倫理審查條件的機構開展委托審查,使我國的倫理委員會機制更加完善。
我國生命科學倫理治理的問題與挑戰
生命科學倫理立法相對滯后,難以及時發揮約束作用。法律法規是政府治理科技倫理的強制性工具,具有剛性約束的作用。我國經過近30 年的發展,雖相繼出臺了《人胚胎干細胞研究倫理指導原則》《涉及人的生物醫學研究倫理審查辦法》《涉及人的生命科學和醫學研究倫理審查辦法(征求意見稿)》等生命科學領域的倫理治理部門規章,相關倫理規范也逐步被寫入《中華人民共和國基本醫療衛生與健康促進法》《中華人民共和國生物安全法》《中華人民共和國刑法》等上位法,但生命科學前沿交叉的學科屬性決定了相關新技術和新問題層出不窮。例如,合成生物學、人工智能等新興領域涉及的倫理問題錯綜復雜,而我國的現有倫理治理法律法規相對滯后,無法及時化解風險和矛盾,多處于“事后止損”階段,呈現出執行力度弱、法律法規不適用等現實問題。
機構倫理委員會監管作用不到位,人力與資金缺乏。在我國建設“國家科技倫理委員會”的大背景下,目前,重點高校相繼建立了自己的科技倫理委員會,對涉人科技倫理、實驗動物倫理等領域開展了針對性監管。但相比美國及歐洲一些國家,倫理審查在我國生命科學領域的科技項目立項與開展中的重要性并未獲得充分的認識,缺乏專門的人員與資金配置,存在人員兼職及審查流于形式等情況;倫理委員會的獨立性未得到充分保障,倫理審查的內容缺乏規范性,后續的跟蹤審查也缺乏持續性,機構層面的監管作用有待進一步提升。
研究人員自律意識不強,需提升倫理培訓。研究人員的倫理治理貫穿了科研的整個流程,從實驗設計、研究實施到結果分析,再到最后的成果發表與成果轉化,整個過程中均應嚴格遵守道德操守和科研倫理。而在聲名、財富和地位等因素的影響下,部分研究人員出現自律意識松懈,倫理價值判斷缺失或偏離,并產生嚴重違背科研倫理的事件,為倫理治理帶來挑戰。此外,我國的高校與研究機構雖然已開展相關的科技倫理培訓,但未建立常態化的倫理與安全培訓、考核機制,未能切實落實培訓的參與度與時效性。
公眾倫理治理參與度低,科普力度有待加強。生命科學技術的倫理治理不僅在于如何對科學研究人員和臨床醫學工作者進行有效引導和管理,還應讓更多的公眾參與進來進行討論。生物技術涉及一些非常敏感的話題,推動其未來在臨床上應用,需要更多的研究以及社會共識。公眾是倫理治理體系的重要組成部分,保證公眾的權益,促進公眾對科學研究和應用的理解已成為重要趨勢。目前,按照倫理委員會人員組成要求,公眾已參與其中;但因缺乏必要的科普培訓,公眾在參與具體事務時不具備相應能力,且積極性不高。科學家作為技術的實際創新人員相比于媒體更能夠客觀、公正地表達技術最“真實”的一面,使公眾對新興技術有全面的認識;但是,基于保密性需要,以及干擾日常科研工作等原因,我國一些科學家并不熱衷于參與科普工作。
關于我國生命科學領域倫理治理的思考與建議
生命科學研究的開展必須受到倫理的規范和引導。倫理制度的建立能夠保證科研創新更有序地開展,保持二者間的張力與平衡,是未來生命科學發展與倫理全面進步的基礎。生命科學領域的倫理治理體系涉及多個利益主體,我國生命科學領域的倫理治理需要考慮到各方的利益與訴求,形成政府、研究機構、科研人員、產業、社會公眾“協同共治”的倫理管理體系。
政府層面:加快構建倫理先行的科技創新體系。政府是生命科學領域倫理治理規則、政策的制定者,應加快構建倫理先行的科技創新體系。面對生命科學領域層出不窮的新興技術風險,政府需在第一時刻分析技術特點,對可能出現的倫理問題主動干預,構想技術應用場景。進而,應研判技術發展趨勢,建立明確的科研倫理法律或規則,在規避生命倫理風險的同時保證科研及臨床轉化工作的順利開展,為高校、研究機構、企業等制定科研倫理規章制度提供指引。可參考英國、德國等國就生命倫理管理建立針對性的法律文件。通過完備的、有強制力的指導性法規,對違反規定的人員與機構建立明確的問責制度,并在一定范圍內賦予倫理管理單位行政主體的資格,對研究人員及科技成果使用者的行為加以約束。將參與國際倫理議題討論和國際倫理規則制定納入建設世界科技強國的重要內容,尤其是倫理爭議大的新興科技領域。提升我國在生命科學倫理治理中的國際話語權,讓中國的倫理思想及話語成為國際倫理治理的重要邏輯組成部分。
機構層面:發揮監督管理主體作用。高校、科研機構、醫療機構是生命科學領域倫理治理的監督與管理者,有權監督科研行為,也有責任堅守倫理規范。“基因編輯嬰兒”事件后,許多高校成立了科技倫理委員會,醫療機構一般設有臨床試驗倫理委員會。為了有效發揮機構監督管理主體的作用,高校、科研機構、醫療機構等均需設立專門部門以加強科技倫理日常管理;并建立常態化工作機制,對機構科技活動的生命倫理風險主動研判、及時化解。此外,機構需加強科學家生命倫理教育培訓,幫助科研人員識別生命科學技術研究和應用中的倫理問題、掌握倫理分析決策的方法,幫助科學家合乎倫理地開展科研活動。
研究人員:加強倫理自治和自我約束。研究人員是生命科學領域倫理治理的關鍵行為者。研究人員需積極履行倫理準則,嚴格遵守國家、地方與機構的科研倫理規章制度。對于尚未建立規章制度的新興生物技術領域,國際社會積極呼吁科學家通過多種類型的自治或自律約束參與治理,充分發揮科學共同體的自治作用和科學傳播作用。同時,樹立良好的科研倫理意識,自覺自律,是研究人員開展倫理自治的關鍵。因此,研究人員需積極參與相關倫理培訓,強化科研誠信,明確個人研究領域的倫理風險與道德責任,增強研究過程的風險防控意識。
行業層面:形成倫理共識有序發展。市場是生命科學領域倫理治理的矛盾中心,很多生命倫理問題的發生根源即在于商業化過程中個人經濟獲益與社會群體福祉的沖突。我國的醫藥產業正處于巨大變革之中,而醫藥產品具有極強的商品性和社會性。因此,行業協會等社會組織作為獨立的第三方,需要積極發揮自身的專業優勢,發揮同行評議和同行監督的作用。由行業協會與企業團體建立行業層面的倫理共識,明確一些生命科學“敏感”地帶的成果轉化路徑與商業化渠道,明確醫藥市場的“倫理紅線”,以從利益產出端約束科研創新行為,促進中國乃至全球醫藥行業健康發展。
公眾層面:共同參與倫理治理生態建設。公眾是生命科學領域倫理治理的見證者與參與者,建設公眾層面共同參與治理的倫理生態至關重要。倫理委員會的倫理審查需要加強對非醫學、非科學委員的倫理培訓,提升非醫學、非科學委員對倫理項目審查的專業性與客觀性。生命科學的倫理治理生態建設需要更加重視“公眾對話”。我國需積極發揮媒體與互聯網在倫理治理中的作用,搭建新興技術與公眾對話的平臺,由科學家、倫理學家、社會學家、研究機構、政府主管部門共同參與,廣泛聽取公眾的意見,鼓勵公眾了解生命倫理,并積極參與科研倫理治理活動,監督并抵制生命科學中的科研失范行為。在科學家層面,科技管理的政府部門需要進一步調動科研人員參與公眾對話與科普工作的積極性,將“科普成就”列入科學家的評估系統,鼓勵科學家從專業層面給予新興生物技術正確地“技術定位”與“輿論導向”。
建立具有“中國特色”的倫理治理體系。由于生命科學領域的倫理治理機制和方法主要是“舶來品”,西方的治理體系雖然提供了有益的視角,但不能完全解決我國面臨的問題。因此,在倫理制度的制定過程中,要考慮到我國的實際國情,根據各地不同的經濟發展基礎與科學發展水平因地制宜、建立健全相關法律法規,規范倫理審查行為。此外,我國的倫理建設還需傳承我國傳統文化中優秀的倫理價值觀,契合我國從古至今“重生”“貴生”或“生命價值”的文化形態,從中國傳統和現實問題出發,揭示并闡述生命科學倫理治理中的中國文化觀點,并將這些觀點融入倫理制度的每一個環節,創造一個滿足科研與產業規范發展且兼備人性溫暖的具有“中國特色”的生命科學倫理治理體系。 (《中國科學院院刊》供稿)
